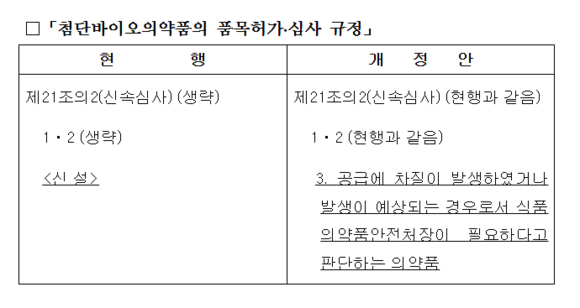
첨단바이오의약품의 품목허가·심사 규정. 사진=식품의약품안전처
식품의약품안전처(처장 오유경)는 백신 등 바이오의약품의 공급 위기를 대비한 신속한 심사 체계 구축을 강화하기 위해 ‘생물학적 제제 등의 품목허가·심사규정’과 ‘첨단바이오의약품의 품목허가·심사규정’을 12일 개정·시행한다.
이번 개정은 5일 발표한 ‘식의약 안심 50대 과제’의 일환으로, 코로나19 상황 등에서 발생할 수 있는 공급 부족 위기 시 우선적으로 심사할 수 있는 대상을 ‘공급 부족 발생 의약품 등 식약처장이 필요하다고 판단하는 의약품’까지 추가·확대해 환자의 치료와 예방 기회를 얻고자 추진됐다.
한편, 식약처는 ‘식의약 안심 50대 과제’의 일환으로 2차 포장의 제조번호가 다르더라도 1차 포장의 제조번호가 동일한 경우에는 국가출하승인을 면제하도록 ‘국가출하승인의약품 지정, 승인 절차 및 방법 등에 관한 규정’ 개정안을 4일 행정예고한 바 있다.
식약처 관계자는 “앞으로도 바이오의약품 관련 규제 개선 과제를 신속하게 추진하며 적극적으로 제도를 개선해 나가겠다”고 말했다.
<문화경제 한시영 기자>





